

Herzlich Willkommen zur PMCF-Konsensbildung!
Sie möchten sich an der Initiative beteiligen?
Wenn Sie Teil der PMCF-Konsensbildung werden möchten, können Sie sich auf dieser Seite ganz einfach für das nächste Folgetreffen in der für Sie relevanten Produktkategorie anmelden.
Wie funktioniert die Anmeldung zu den Treffen?
In der nachfolgenden Tabelle finden Sie eine Übersicht zu allen gebildeten Produktgruppen. Unter "Nächster Termin" können Sie sehen, für welches Datum das nächste Folgetreffen der jeweiligen Produktgruppe geplant ist. Anschließend können Sie sich unter "Terminbuchung" für die einzelnen Treffen anmelden. Klicken Sie dazu einfach auf "Anmeldungslink". Der Link leitet Sie weiter zu einem Anmeldeformular, in welches Sie bitte Ihren Namen, den Namen ihres Unternehmens, sowie Ihre E-Mail Adresse eintragen.
Nachdem Sie das Formular vollständig ausgefüllt haben, werden Sie automatisch in den Verteiler der jeweiligen Produktkategorie aufgenommen. Sobald ein neuer Termin feststeht, erhalten Sie automatisch eine Einladung zum Treffen, welchen Sie dann in Ihren persönlichen Kalender übernehmen können.
Aktuelle Terminübersicht
Aktive Produktkategorien
In dieser Tabelle finden Sie eine Übersicht der Produktkategorien, in denen aktuell in regelmäßigen Abständen Treffen stattfinden.
Produktkategorie |
Moderatoren |
Nächster Termin |
Terminbuchung |
|---|---|---|---|
|
Produktkategorie L |
Marena Hauser Meinrad Kempf |
Folgetermin Plattform |
Anmeldung |
|
Produktkategorie P
|
Dr. Andreas Halbleib Saskia Mathieu Prof. Dr. Andreas Nüssler Prof. Dr. Arndt-Peter Schulz Frank Trautwein |
Folgetermin Aktuell finden keine Treffen in dieser Produktkategorie statt. Plattform
|
Anmeldungslink |
Aktive Produktkategorien
In dieser Tabelle finden Sie eine Übersicht der Produktkategorien, in denen aktuell keine Treffen stattfinden. Eine Reaktivierung dieser Gruppen ist jedoch zeitnah geplant. Sie können sich bereits jetzt registrieren und erhalten eine Benachrichtigung, sobald wieder Treffen stattfinden.
Produktkategorie |
Moderatoren |
Nächster Termin |
Terminbuchung |
|---|---|---|---|
|
Produktkategorie J |
Tobias Barth |
Folgetermin Plattform |
Vorregistrierung Sobald es wieder einen Termin gibt, werden Sie automatisch benachrichtigt. |
|
Produktkategorie K |
Dr. Andreas Halbleib |
Folgetermin Plattform
|
Vorregistrierung Sobald es wieder einen Termin gibt, werden Sie automatisch benachrichtigt. |
|
Produktkategorie N |
Dr. Andreas Halbleib |
Folgetermin Plattform |
Vorregistrierung Sobald es wieder einen Termin gibt, werden Sie automatisch benachrichtigt. |
|
Produktkategorie Q |
Dr. Franziska Bursch Dr. Andriani Daskalaki |
Folgetermin Plattform |
Vorregistrierung Sobald es wieder einen Termin gibt, werden Sie automatisch benachrichtigt. |
|
Produktkategorie S |
Dr. Franziska Bursch (COLTENE AG) |
Folgetermin Plattform |
Vorregistrierung Sobald es wieder einen Termin gibt, werden Sie automatisch benachrichtigt. |
|
Produktkategorie U |
Elena Scheller (Karl Storz) |
Folgetermin Plattform |
Vorregistrierung Sobald es wieder einen Termin gibt, werden Sie automatisch benachrichtigt. |
|
Produktkategorie V |
Dr. Andriani Daskalaki Robert Radloff |
Folgetermin Plattform |
Vorregistrierung Sobald es wieder einen Termin gibt, werden Sie automatisch benachrichtigt. |
|
Produktkategorie W |
Robert Radloff |
Folgetermin Plattform |
Vorregistrierung Sobald es wieder einen Termin gibt, werden Sie automatisch benachrichtigt. |
|
Produktkategorie Y |
Lukas de Hond |
Folgetermin Plattform |
Vorregistrierung Sobald es wieder einen Termin gibt, werden Sie automatisch benachrichtigt. |
|
Produktkategorie Z |
Dr. Andriani Daskalaki |
Folgetermin Plattform |
Vorregistrierung Sobald es wieder einen Termin gibt, werden Sie automatisch benachrichtigt. |
Sie können keine für Sie relevante Produktkategorie oder -gruppe identifizieren?
Dann kontaktieren Sie uns bitte unter pmcf-consensus@raylytic.com. Gerne helfen wir Ihnen bei der Gründung neuer Produktkategorien oder -gruppen.
European Medical Device Nomenclature (EMDN)
Bedeutung und Struktur des EMDN-Katalogs
Im Rahmen der Konsensbildung, orientiert sich die Initiative an dem EMDN-Katalog der Europäischen Kommission.
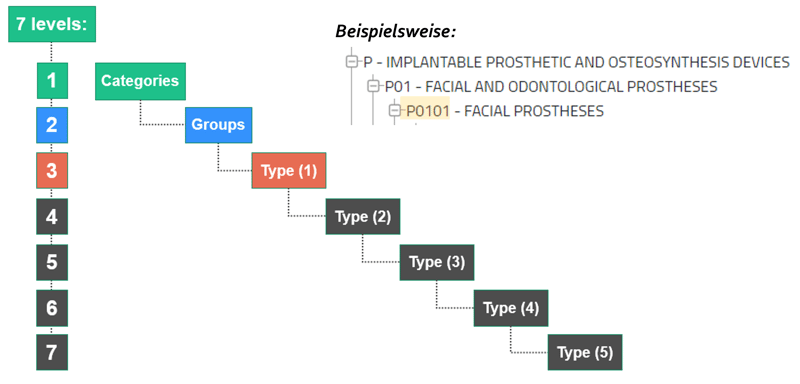
Die EMDN zeichnet sich durch seine alphanumerische Struktur aus, die in einem siebenstufigen hierarchischen Baum aufgebaut ist. Dieser gruppiert Medizinprodukte in drei Hauptebenen:
-
- Kategorien: die erste hierarchische Ebene,
- Gruppen: die zweite hierarchische Ebene,
- Typen: die dritte hierarchische Ebene (die sich gegebenenfalls in mehrere Detailebenen aufgliedert).
Zugriff zum EMDN-Katalog erhalten Sie unter folgendem Link: EMDN-Katalog.
Viele Akteure – eine gemeinsame Vision
Das Konsortium aus 16 etablierten Organisationen der Medizintechnik, Pharmaindustrie und Gesundheitsversorgung gewann 2019 unter dem Projekt-Akronym „KIKS“ den KI-Wettbewerb der Bundesregierung. Seit Januar 2020 entwickeln die Partner des vom BMWi geförderten Projekts die technische Infrastruktur und darauf aufbauende Anwendungen. Im Zentrum steht die datenschutzkonforme, anonymisierte Bereitstellung strukturierter medizinischer Daten für Prozessautomatisierung, Studien, Forschung und Produktentwicklung. Besonderes Merkmal des Projekts ist die enge Kooperation zwischen Industrie, Forschung und Versorgungseinrichtungen.
Innovationen datengestützt und automatisiert vorantreiben
Für technologische Entwicklungen im Gesundheitswesen ist es entscheidend, medizinische und klinische Daten hoher Qualität in einem austauschbaren, kontextbewahrenden Format bereitzustellen, von dem aus ein datenschutzkonformer Zugriff der verschiedenen Stakeholder wie Klinik, Forschung, Medizintechnik und Pharmazie sichergestellt ist. AIQNET macht klinische Daten aus Labor, Radiologie, Anamnese, Diagnose und Behandlungsverlauf über ein System zugänglich. Die rechtlichen und ethischen Rahmenbedingungen für die Verarbeitung medizinischer Daten zu Forschungszwecken werden mittels eines Governance-Frameworks vollumfänglich umgesetzt und Patienten weitreichende Kontrollmöglichkeiten eingeräumt.
AIQNET unterstützt Sie bei klinischen Prüfungen und Studien
Um die Planung und Durchführung von klinischen Prüfungen und Studien zu vereinfachen, ermöglicht AIQNET die Nutzung strukturierter klinischer Daten, unabhängig von Systemen, Schnittstellen und Organisationen. Das Ökosystem bietet die technologische Infrastruktur für Big-Data-Analysen, den Zugriff auf Real World Daten und kann damit auch Bedarfe zur Entwicklung von KI-Anwendungen abdecken. Mit dem bereits verfügbaren Clinical Trial Management System lassen sich umfangreiche Analyse- und Auswertefunktionen, E-Mail-Benachrichtigungen, risikobasiertes Monitoring und intuitive Dashboards kostengünstig, transparent und effizient automatisieren sowie unter Einbeziehung aller Stakeholder planen, überwachen und analysieren.
Reduktion des Integrations- und Entwicklungsaufwands für neue Klinikanwendungen
Mit der Inbetriebnahme von AIQNET lassen sich eine Vielzahl an Applikationen ohne zusätzlichen Integrationsaufwand aus der Plattform heraus bereitstellen. Auch Softwarehersteller und Hersteller digitaler Gesundheitsanwendungen (DiGAs) können die in Bezug auf Datensicherheit und Datenschutz unabhängig validierte Plattform zur Implementierung ihrer Anwendung nutzen.
Ziel ist es, den Digitalisierungsprozess ohne Integrationsschranken auf Basis des FHIR-Standards voranzutreiben. Der Zugang zu kompatiblen Anwendungen von Drittanbietern erfolgt über einen Marktplatz und bietet Pharmazeutika- und Medizintechnikherstellern die Möglichkeit, hochspezialisierte Anwendungen, z. B. für datenbasierte Diagnostikverfahren, deutlich schneller zu entwickeln, in den klinischen Workflow zu integrieren und somit in die Anwendung zu bringen.

